在全球和中國醫藥市場(chǎng)上���,抗體藥物已連續多年占據銷(xiāo)售榜單前幾位��。當前�����,隨著(zhù)國家醫改政策的改革和完善����,國際�����、國內市場(chǎng)打通��,抗體市場(chǎng)也開(kāi)始進(jìn)入“你方唱罷我登場(chǎng)”群雄逐鹿的競爭階段�,生產(chǎn)企業(yè)如何在確保產(chǎn)品質(zhì)量的基礎上�,通過(guò)改進(jìn)工藝�,來(lái)降低成本��、提高生產(chǎn)效率和市場(chǎng)競爭力���?江博士文章給讀者提供了一條切實(shí)可行的思路和方法���,請看“如何突破抗體生產(chǎn)瓶頸”����。

關(guān)于抗體藥物市場(chǎng)及發(fā)展趨勢
全球生物制藥產(chǎn)業(yè)發(fā)展迅猛��,根據Frost&Sullivan市場(chǎng)調研�����,2018年全球生物制藥市場(chǎng)規模約為2642億美元���。單抗類(lèi)藥物由于特異性好�����,靶向性高��,副作用小�,療效顯著(zhù)成為發(fā)展最快的一類(lèi)生物藥����。單抗藥物在全球生物藥中所占市場(chǎng)份額超過(guò)50%����,達到1353億美金���。
中國巨大的市場(chǎng)潛力�,國際重磅抗體藥專(zhuān)利到期��,大量的海歸人才回流及中國日益強大的資本助力��,都為中國抗體制藥發(fā)展提供了前所未有的歷史機遇�。但是中國抗體制藥企業(yè)也面臨巨大的挑戰���。首先中國藥企無(wú)論是技術(shù)�����、規模�����、經(jīng)驗���,人才還是資金�����,跟國際生物制藥巨頭相比�,都有著(zhù)較大的差距���。其次中國加入ICH和國際藥監管體系接軌�����,降低藥品進(jìn)口關(guān)稅����,對進(jìn)口抗癌藥物實(shí)施零關(guān)稅等系列政策�����,降低了國外原研藥進(jìn)入中國市場(chǎng)的門(mén)檻��,給中國生物藥企業(yè)帶來(lái)了巨大壓力和挑戰��。另外�����,越來(lái)越多的制藥企業(yè)進(jìn)入抗體藥的開(kāi)發(fā)領(lǐng)域�����,每個(gè)重磅抗體藥物基本上都有幾十家企業(yè)在仿制研發(fā)申報�����,因此國內抗體藥企不僅要面臨國外原研藥巨頭的打壓�����,還要面對國內眾多同行及印度廉價(jià)藥企業(yè)激烈的競爭���。最后帶量采購新政允許通過(guò)一致性評價(jià)的仿制藥與原研藥可以一起同臺競標���,低價(jià)中標�����,消除了銷(xiāo)售渠道的壁壘使得國內外生物藥企的競爭回歸到技術(shù)創(chuàng )新�,產(chǎn)品質(zhì)量和成本的競爭����。?因此國內生物藥企是否能在激烈的競爭中取得優(yōu)勢取決于其生產(chǎn)工藝的先進(jìn)性���,因為制藥工藝水平?jīng)Q定了產(chǎn)品的質(zhì)量和成本�����。
關(guān)于抗體藥物的生產(chǎn)工藝進(jìn)展
抗體藥物生產(chǎn)是個(gè)非常復雜的過(guò)程���,大致分為上游的發(fā)酵及下游的分離純化:上游工藝主要包括細胞復蘇���、傳代����、發(fā)酵生產(chǎn)���。而下游工藝主要包括膜過(guò)濾及多步層析分離純化���。過(guò)去十多年來(lái)����,基因工程獲得突飛猛進(jìn)的進(jìn)步�,細胞培養的表達量從原來(lái)的不到0.5 g/L 到現在普遍達到5g/L����,有的甚至超過(guò)10g/L��。這些進(jìn)步是由細胞表達載體的開(kāi)發(fā)�����,克隆篩選以及細胞培養基優(yōu)化等技術(shù)創(chuàng )新所驅動(dòng)的�����。由于發(fā)酵產(chǎn)率的大幅度提升����,使得上游細胞培養成本大幅度降低(表1)��。
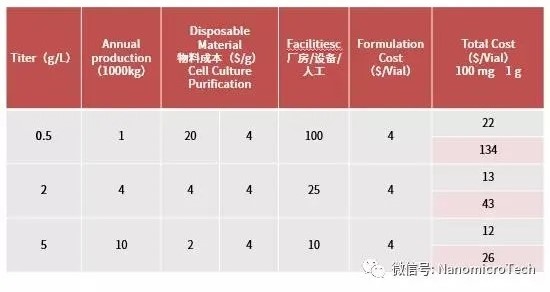
表1??表達量與抗體生產(chǎn)成本關(guān)系
與上游十多倍生產(chǎn)效率提升相比����,下游分離純化技術(shù)進(jìn)步明顯滯后���,導致下游工序成為生產(chǎn)瓶頸��,抗體主要生產(chǎn)成本也轉移到下游��。下游工藝在整個(gè)生物制藥生產(chǎn)中占據60%以上生產(chǎn)成本���,也被認為是最需要改進(jìn)的技術(shù)領(lǐng)域�����。下游工藝先進(jìn)性決定了藥品的質(zhì)量�����,及藥品生產(chǎn)效率和成本�,也成為生物制藥企業(yè)的核心競爭力所在�����。
生物制藥下游生產(chǎn)工藝目的就是把目標藥物分子從復雜發(fā)酵液體系中分離出來(lái)以滿(mǎn)足藥品純度及質(zhì)量的需求��。一方面監管部門(mén)對生物藥的純度和質(zhì)量要求越來(lái)越高�,另一方面生物分子具有結構復雜��,且對外部條件敏感�����,穩定性差���,雜質(zhì)多��,濃度低等特點(diǎn)����,使得生物藥分離純化的挑戰更大��。比如說(shuō)治療用抗體不僅對含量有嚴格的要求����,還必須去除各種潛在的雜質(zhì)如宿主HCP, DNA�����,Endotoxin, 抗體聚集體及降解片段等(表2)�����。

表2 ?抗體藥物對各種雜質(zhì)的要求
層析技術(shù)具有分離純化效率高����,條件溫和且容易保持目標分子的生物活性��,因此成為生物制藥分離純化最主要工具��。但下游層析分離純化技術(shù)牽涉到材料���、生物����、化學(xué)及設備等交叉技術(shù)領(lǐng)域��。因此研究下游分離純化技術(shù)的人才較少��,另外上游基因工程技術(shù)幾乎在所有高校都有專(zhuān)業(yè)研究團隊���,而且培養了大量的人才�����,而下游分離純化技術(shù)卻很少在高校有專(zhuān)門(mén)研究���,也缺乏相關(guān)的專(zhuān)業(yè)課程來(lái)培養分離純化的人才��。過(guò)去10多年上游基因工程的迅猛發(fā)展雖然帶來(lái)上游發(fā)酵成本的大幅度下降����,但下游分離純化技術(shù)進(jìn)步緩慢使其成本居高不下�。因此要降低抗體生產(chǎn)成本關(guān)鍵就是要解決下游分離純化的瓶頸問(wèn)題���。
抗體的層析分離步驟基本都可以采用標準化的三步曲:第一步用Protein A介質(zhì)進(jìn)行抗體捕獲和濃縮���;第二步用離子交換進(jìn)行中間純化以去除多聚體�����,宿主蛋白等雜質(zhì)�����;第三步是精純去除剩余DNA��,Endotoxin,Protein A 等微量雜質(zhì)��。在這三步抗體的分離純化過(guò)程中��,第一步的Protein A親和捕獲占據分離純化成本80%以上���,也是下游分離純化的瓶頸所在�����。親和層析之所以成本高的主要原因:首先是Protein A 價(jià)格昂貴��,其價(jià)格是普通層析介質(zhì)十幾倍�;第二���,Protein A使用壽命短�����,一般離子交換填料使用壽命多達1000次���,而親和填料壽命通常在100-200次����;第三��,Protein A 用于抗體的捕獲和濃縮���,需要處理大體積的發(fā)酵液���,而親和步驟載量往往又低于陰陽(yáng)離子交換層析�����,使得親和層析介質(zhì)使用量比中間純化或精純的要多得多��。因此�,要降低抗體的生產(chǎn)成本��,解決抗體的生產(chǎn)瓶頸關(guān)鍵在于改進(jìn)第一步Protein A 親和捕獲��。

下游分離純化核心的工藝流程
Protein A 親和層析是利用Protein A 配基與目標抗體具有專(zhuān)一親和吸附作用從而達到分離純化抗體的目的�����。野生型Protein A蛋白是金黃色葡萄球菌細胞壁錨釘蛋白�。三維空間上�,抗體FC端CH2-CH3區域與Protein A蛋白B結構域上兩條反相平行的α螺旋結構相互結合�����。因此Protein A與抗體分子特別是與IgG1���、IgG2����、IgG4有特異性結合��,使得抗體分子與發(fā)酵液中不具FC端結構的雜質(zhì)如宿主蛋白與核酸等有效分離����,進(jìn)而達到純化目的���。Protein A 親和層析介質(zhì)是通過(guò)把ProteinA 配基偶聯(lián)到微球介質(zhì)上制備而成的���。因為Protein A配基與目標抗體的作用的專(zhuān)一性�����,因此親和層析的分離純化工藝和方法與抗體樣品雜質(zhì)含量和種類(lèi)多少影響不大�,使用Protein A 介質(zhì)一步純化目標抗體就可以達到95%以上純度��,回收率達到90%以上���。親和純化效率也基本不受雜質(zhì)多少影響��,而其它分離模式如離子交換���,疏水�����,分子篩等的分離工藝方法及效率大多取決于與目的蛋白同時(shí)存在的雜質(zhì)種類(lèi)和含量��。因此��,只要樣品雜質(zhì)不同����,即使是純化同樣的目標生物分子���,采用的分離工藝和方法就不同�。以重組胰島素分離純化為例�,不同廠(chǎng)家雖然生產(chǎn)的是同一目標胰島素�,但采用分離純化方法完全不一樣�,主要原因就是每家生產(chǎn)的胰島素雜質(zhì)組成和含量不一樣�����,因此需要不同的純化工藝���。而比胰島素分子量更大���,結構更復雜的抗體基本可以采用標準化的三步曲����,主要原因就是Protein A 親和介質(zhì)的出現大大簡(jiǎn)化抗體的分離純化工藝���,但Protein A 價(jià)格昂貴讓抗體生產(chǎn)廠(chǎng)家愛(ài)恨交加���。
Protein A 介質(zhì)價(jià)格高的主要原因是其生產(chǎn)工藝復雜�,ProteinA 配基是通過(guò)生物發(fā)酵生產(chǎn)的���,經(jīng)過(guò)純化后偶聯(lián)到介質(zhì)上成為Protein A 親和介質(zhì)�,因此生產(chǎn)成本遠高于傳統的離子交換���、疏水����、分子篩等介質(zhì)��。另一方面Protein A產(chǎn)品主要由歐美幾家供應商壟斷���,也是價(jià)格居高不下的原因之一����。為了降低抗體生產(chǎn)成本��,不少研究工作者在尋找可以取代Protein A且價(jià)格低廉的新型層析介質(zhì)來(lái)純化抗體�,雖然可能在一些個(gè)案中獲得成功����,但都無(wú)法撼動(dòng)Protein A 在整個(gè)抗體分離純化的壟斷地位���。ProteinA 親和層析成為過(guò)去近30年里抗體純化捕獲的金標準��。因此要降低抗體親和層析這一步的成本首要的方案是實(shí)現Protein A 介質(zhì)的國產(chǎn)化以降低產(chǎn)品價(jià)格��;其次是通過(guò)采用創(chuàng )新的連續層析工藝技術(shù)或其它新工藝以提高Protein A 介質(zhì)的利用率并提高抗體生產(chǎn)效率����。當然不斷改進(jìn)Protein A 介質(zhì)性能使其具有更高的載量和更長(cháng)的使用壽命也可以降低抗體的生產(chǎn)成本�。
Protein A介質(zhì)國產(chǎn)化創(chuàng )新之路
目前市場(chǎng)上主流Protein A產(chǎn)品是GE生產(chǎn)的以瓊脂糖為基質(zhì)的產(chǎn)品���,也是最早商業(yè)化的產(chǎn)品���。瓊脂糖為基質(zhì)的Protein A 介質(zhì)具有載量高�����,親水性能好��,非特異性吸附低等優(yōu)點(diǎn)�����,但瓊脂糖介質(zhì)天然缺陷是機械強度差�,因此也被稱(chēng)為軟膠��。由于該介質(zhì)耐壓性能差���,生產(chǎn)中需要降低柱高����、減小流速以防止壓力過(guò)高造成柱床塌陷��,限制了抗體批處理量及抗體生產(chǎn)效率���。軟膠Protein A 另外一個(gè)缺陷是傳質(zhì)速度慢����,主要原因是軟膠孔徑較小����,排阻大�。因此軟膠Protein A 都需要駐保留時(shí)間長(cháng)����,流速慢條件下��,抗體吸附載量才會(huì )比較高�,但在高流速下動(dòng)態(tài)載量下降的非?����??。因此一個(gè)理想的抗體純化用Protein A 介質(zhì)需要具有高流速����,高載量�����,高機械強度��,及更長(cháng)的使用壽命等特點(diǎn)�����。Protein A 介質(zhì)載量是由微球孔徑����,比表面積�����,配基密度來(lái)決定的��;機械強度則是由Protein A基球材料化學(xué)組成���,交聯(lián)度及孔隙率來(lái)決定的�����;Protein A 配基脫落及使用壽命主要由配基�,基球性能及偶聯(lián)方式來(lái)決定�。實(shí)現高性能Protein A 親和介質(zhì)的國產(chǎn)化需要從底層創(chuàng )新開(kāi)始����。
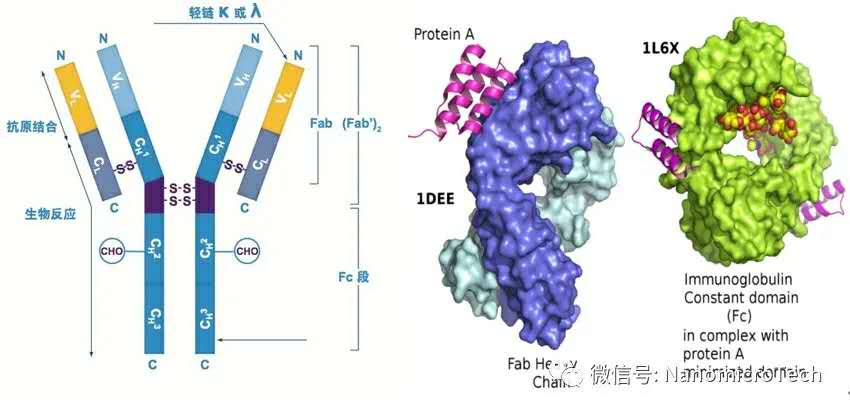
抗體結構示意圖
創(chuàng )新之一:?jiǎn)畏稚⒒蛱娲喾稚⒒?/span>
層析介質(zhì)粒徑大小和粒徑分布是影響層析分離的重要參數�。粒徑分布越均勻�����,裝柱越容易����、柱床越穩定�、柱效越高���、流速越均勻���、洗脫越集中��、分離效率越高��、流動(dòng)相用量越少��,柱與柱重復性也越好����;Protein A 介質(zhì)被譽(yù)為層析介質(zhì)皇冠上的明珠���,價(jià)格昂貴��,可是市場(chǎng)上Protein A 介質(zhì)都是采用粒徑分布較寬的基球�。主要原因是單分散微球制備技術(shù)難度極大����,世界上可以規模生產(chǎn)的單分散多孔微球只有Dynal公司一家�����,GE銷(xiāo)售的SOURCE 系列單分散聚苯乙烯色譜填料就是Dynal生產(chǎn)的���。但SOURCE 產(chǎn)品的粒徑最大只有30微米���,不能滿(mǎn)足Protein A 介質(zhì)對粒徑一般要大于40微米的要求�����。納微經(jīng)過(guò)多年的努力開(kāi)發(fā)出世界領(lǐng)先的微球精準制備技術(shù)�����,突破大單分散大粒徑多孔微球的制備難題�����,成為全球第一家生產(chǎn)單分散Protein A 親和層析介質(zhì)的公司����。

納微單分散Protein A介質(zhì)與傳統軟膠基質(zhì)微觀(guān)結構對比
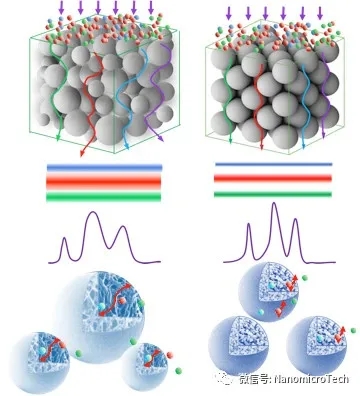
傳統多分散Protein A親和軟膠與UniMab液流路徑對比示意圖
創(chuàng )新之二:通透大孔徑基球微替代小孔微球
Protein A 基球孔徑大小會(huì )影響生物分子在介質(zhì)的傳質(zhì)速度和有效載量��,孔徑越大��,分子傳質(zhì)速度越快�,在高流速下具有高載量���?�;谲浤z基質(zhì)的GE Protein A親和介質(zhì)孔徑較小���,比表面積高����,其靜態(tài)吸附載量高��,但傳質(zhì)阻力大����,在駐留時(shí)間短�����,流速快的條件下���,動(dòng)態(tài)載量下降的很快�����。納微經(jīng)過(guò)優(yōu)化篩選���,專(zhuān)門(mén)設計的大孔結構基球�,其孔徑達到GE Protein A 介質(zhì)的一倍左右���。因此該介質(zhì)傳質(zhì)速度快����,使得介質(zhì)在高流速下具有高載量��。從實(shí)驗測試數據可以看到���,納微UniMab與GE MabSelectSuRe在駐留時(shí)間大于4分鐘時(shí)�,載量都差不多���,當駐留時(shí)間小于2分鐘時(shí)UniMab的載量比MabSelectSuRe載量高50%以上, 而且速度越快UniMab載量?jì)?yōu)勢越明顯��??贵w生產(chǎn)效率是由動(dòng)態(tài)載量和流速共同決定�,流速越快載量越高�����,生產(chǎn)效率越高�����,成本越低���,但親和層析介質(zhì)的動(dòng)態(tài)載量與流速成反比��,流速越快��,載量越低�����,因此對于每個(gè)Protein A親和介質(zhì)純化抗體效率都會(huì )隨著(zhù)流速升高效率逐步提高��,到了一個(gè)最優(yōu)的流速后�����,如果繼續增加流速��,純化效率反而降低�。林東強教授實(shí)驗證明對于批次親和層析�����,駐留時(shí)間是2分鐘時(shí)生產(chǎn)效率達到最高��,而駐留時(shí)間在2分鐘條件�����,UniMab的動(dòng)態(tài)載量比MabSelectSuRe 高50%以上�����。對于連續層析駐留時(shí)間是1分鐘時(shí)生產(chǎn)效率最高�,而這個(gè)保留時(shí)間�,UniMab的動(dòng)態(tài)載量更是MabSelectSuRe一倍以上�。另外從抗體流穿曲線(xiàn)對比圖也可以看出具有大孔結構及高度粒徑均勻性的單分散Protein A親和層析介質(zhì)與多分散軟膠PorteinA 介質(zhì)相比具有更陡的穿透曲線(xiàn)���,說(shuō)明納微單分散層析介質(zhì)具有更暢通的孔道結構�,分子擴散速度快��,抗體流穿少�,回收率高���。因此利用納微大孔結構微球不僅可以提高分子傳質(zhì)速度�����,提高抗體生產(chǎn)效率��,降低成本�,而且在連續層析中�,具有更明顯的優(yōu)勢�。
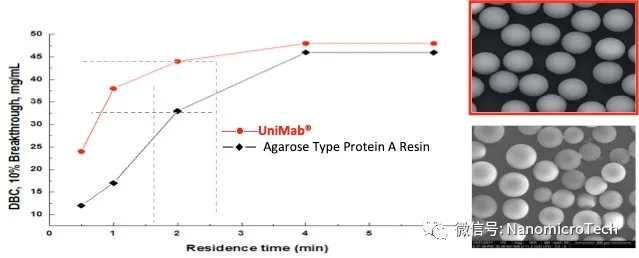
UniMab與MabSelectSuRe產(chǎn)品不同駐留時(shí)間動(dòng)態(tài)載量對比
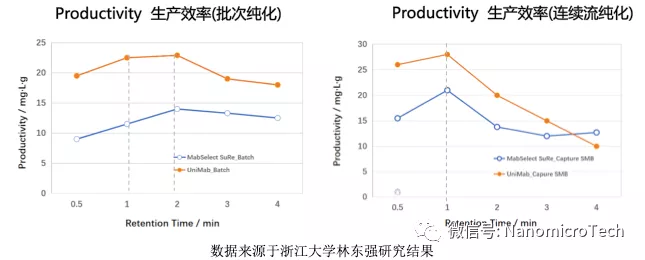
不同Protein A 層析介質(zhì)駐留時(shí)間與抗體生產(chǎn)效率與關(guān)系對比
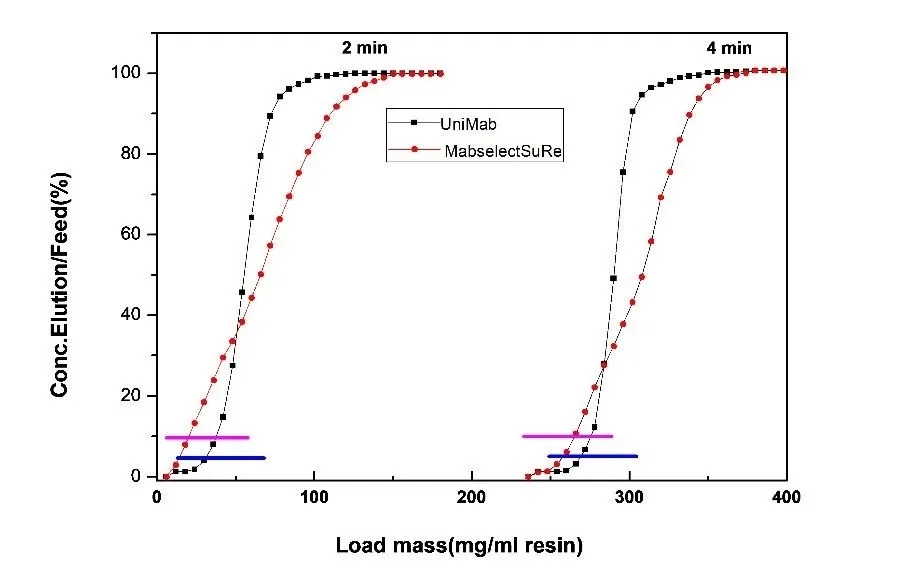
抗體流穿曲線(xiàn)對比圖
創(chuàng )新之三:高度交聯(lián)聚丙烯酸酯基球替代軟膠或低交聯(lián)的聚丙烯酸酯基球
高機械強度介質(zhì)不僅可以耐受更高流速��、更高壓力�����、更大粘度樣品���,還可以裝更高的柱床����,以增加抗體批處理量��、提高抗體生產(chǎn)效率���、減少設備投資�����、減少廠(chǎng)房占用面積�����。因此納微Protein A 介質(zhì)是選擇高度交聯(lián)的聚丙烯酸酯基球���,與市場(chǎng)上以瓊脂糖或低交聯(lián)度聚丙烯酸酯為基球生產(chǎn)的Protein A 介質(zhì)相比具有溶脹系數小���、壓縮比例低�����、而且機械性能強����。實(shí)驗證明 UniMab在2公斤裝柱壓力下����,其柱床壓縮比例只有5%�,而無(wú)論是GE 生產(chǎn)的以瓊脂糖為基球還是Tosoh 生產(chǎn)的低交聯(lián)聚合物為基球的Protein A 介質(zhì)壓縮比例往往超過(guò)15%��。
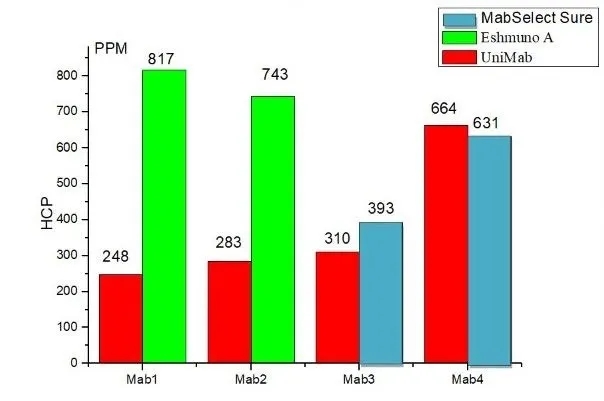
納微UniMab與對照填料的HCP去除效果
創(chuàng )新之五:Protein A 配基創(chuàng )新
除了基球之外�����,Protein A 配基也是影響介質(zhì)性能重要因素�����,尤其是介質(zhì)的壽命���。GE之所以壟斷Protein A 親和層析介質(zhì)市場(chǎng)�����,最主要的是GE擁有耐堿性Protein A 專(zhuān)利技術(shù)�,其核心專(zhuān)利技術(shù)是通過(guò)基因工程改變B domain 不耐堿的3個(gè)氨基酸以改善其耐堿性能�。納微通過(guò)優(yōu)化組合不同片段設計出新序列的Protein A 配基���,不僅耐堿性好����,而且具有自主知識產(chǎn)權��,并能自主實(shí)現大規模生產(chǎn)���。納微獨有的耐堿性配基加上具有卓越性能的基球���,及優(yōu)化偶聯(lián)工藝開(kāi)發(fā)出高性能的Protein A 親和介質(zhì)����。以下是某單抗項目上UniMab介質(zhì)載量隨使用次數增加的衰減變化表�。每個(gè)cycle采用0.1M氫氧化鈉CIP���,接觸時(shí)間1小時(shí)�。連續200個(gè)cycle 后DBC10%依然在初始值的75%左右��,充分體現了納微ProteinA介質(zhì)的良好耐堿性�����。
納微世界領(lǐng)先的微球精準制造技術(shù)�����,可以對微球的材料組成����、粒徑大小��、粒徑均勻性�����、孔徑大小及表面性能達到前所未有的精準控制���。納微利用這一技術(shù)平臺開(kāi)發(fā)出新一代單分散多孔聚丙烯酸酯為基質(zhì)的Protein A 親和層析介質(zhì)克服了傳統ProteinA 軟膠的缺點(diǎn)��,也為實(shí)現下一代連續層析技術(shù)產(chǎn)業(yè)化提供理想的介質(zhì)��。

UniMab載量隨使用次數增加的衰減變化表??
Protein A介質(zhì)創(chuàng )新和生產(chǎn)工藝創(chuàng )新實(shí)現抗體生產(chǎn)效率提升
單抗藥物的市場(chǎng)競爭越來(lái)越激烈����,降低抗體生產(chǎn)成本��,高效�、穩定的產(chǎn)出合格的產(chǎn)品是每個(gè)抗體生產(chǎn)廠(chǎng)家追求的目標����。親和層析作為單克隆抗體分離純化的關(guān)鍵步驟����,關(guān)系到下游的主要成本及生產(chǎn)效率���,產(chǎn)品質(zhì)量����,也是目前下游生產(chǎn)的主要瓶頸�����。因此納微通過(guò)底層技術(shù)創(chuàng )新不僅實(shí)現Protein A 介質(zhì)的國產(chǎn)化����,而且克服了現有產(chǎn)品的缺陷���,必將大幅度提供抗體生產(chǎn)效率���,降低抗體生產(chǎn)成本���,更重要的是納微創(chuàng )新性單分散層析介質(zhì)可以推動(dòng)下游工藝技術(shù)的創(chuàng )新和進(jìn)步�����。比如說(shuō)高機械強度的Protein A 介質(zhì)就使得通過(guò)增加柱床提高批處理量成為可能�。而高流速下的高載量及耐高壓特性為最終實(shí)現抗體連續層析工藝打下基礎��。
1.高柱床提高抗體批處理量和生產(chǎn)效率
目前GE 生產(chǎn)的Protein A 軟膠占據抗體分離純化的90%市場(chǎng)����。由于軟膠機械強度差���,耐壓受限(壓力小于3公斤)�,為了防止柱床塌陷���,一般柱床只裝到15cm高度���,嚴重限制抗體的生產(chǎn)效率����,增加抗體的生產(chǎn)成本�。柱床高不僅可以增加抗體的批處理量���,提供抗體的生產(chǎn)效率�����,還可以減少QA及QC等配套人員的工作量�����,減少純化系統的數量及設備投資�����。其實(shí)���,通過(guò)高柱床提高生產(chǎn)效率的方法早在成本更加敏感的胰島素����、白蛋白����、多肽等生物藥生產(chǎn)上成功實(shí)現�。但要增加柱床高度���,Protein A 介質(zhì)必須具有高機械強度性能��,以滿(mǎn)足高柱床高流速下產(chǎn)生的壓力��。納微開(kāi)發(fā)的新一代單分散Protein A 介質(zhì)是以高交聯(lián)的單分散聚丙烯酸酯為基質(zhì)�,機械強度高���,耐壓性能好���。因此柱床可以裝到40cm以上高度�,使得抗體批處理量及生產(chǎn)效率可以提高一倍以上�,不僅減少設備投資及廠(chǎng)房的占用面積���,而且大幅度降低生產(chǎn)成本�����。另外實(shí)驗證明提高柱床還可以提高介質(zhì)有效載量和利用率��,柱床提高一倍����,抗體上樣量至少增加2.2倍(見(jiàn)表)���。高柱床可以解決因為上游發(fā)酵規模的擴大及蛋白表達量的增加而帶來(lái)下游分離純化生產(chǎn)瓶頸的問(wèn)題���。另外軟膠放大往往只能通過(guò)等高放大�����,而納微生產(chǎn)的高機械強度Protein A 可以等保留時(shí)間放大���。
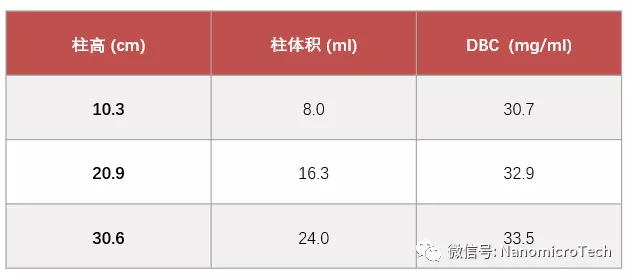
表UniMab對某抗體DBC5%比較

UniMab在不同柱高下的壓力流速曲線(xiàn)
2.連續層析提高抗體生產(chǎn)效率
隨著(zhù)細胞培養技術(shù)的迅猛發(fā)展����,蛋白表達量不斷增加以及新興的連續灌流培養技術(shù)的發(fā)展對下游純化效率提出越來(lái)越高的要求��。批次層析越來(lái)越難以滿(mǎn)足生產(chǎn)的需求�,而連續層析由多根串聯(lián)的層析柱組成��,因為第二根柱子可以承接并吸附從第一根層析柱流穿的抗體���,因此第一根柱子可以持續上樣到更高的蛋白穿透從而顯著(zhù)提高層析柱的使用載量���,進(jìn)而提高介質(zhì)利用率�,降低生產(chǎn)成本��。連續層析可以極大提高設備的利用率����,縮短生產(chǎn)周期���,還可以減少緩沖液的消耗�����。
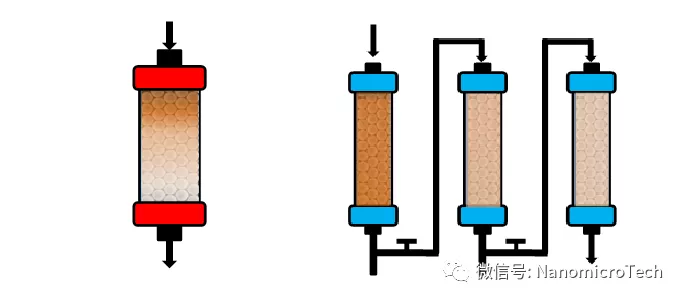
傳統間歇式層析(左)
新型連續層析工藝(右)

連續流層析分離過(guò)程示意圖
(來(lái)源于林東強教授課題組文章)
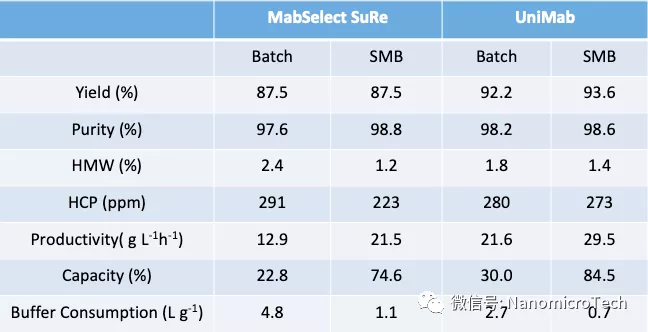
UniMab與MabSelectSuRe在批次與連續層析的對比數據
(來(lái)源于林東強教授課題組文章)
連續層析系統已被認為是下游分離純化的發(fā)展必然趨勢��,可以大幅度提高抗體下游分離純化效率����,降低生產(chǎn)成本�����。與批次層析相比����,連續層析對設備��、軟件有更高的要求���,而且對介質(zhì)的要求也不一樣����。
首先���,連續層析由多根串聯(lián)的層析柱組成����。為了保障產(chǎn)品連續生產(chǎn)的質(zhì)量�,對每根柱子的一致性要求高�。因此介質(zhì)填料均勻性就顯得更為重要��,因為介質(zhì)越均勻��,越容易裝柱子�,柱效也越高�����,柱與柱之間的一致性也越好��。傳統多分散介質(zhì)由于顆粒有大有小���,在裝柱過(guò)程中大小顆粒的沉降速度不同����,使得柱與柱之間差異較大�;而且小顆粒容易堵塞篩板�����,影響流速�����,大顆粒又會(huì )降低柱效�����,也容易使樣品流穿���,從而影響分離效率�����。因此高度粒徑均一的單分散層析介質(zhì)可以克服傳統多分散介質(zhì)在連續生產(chǎn)中存在的問(wèn)題���,單分散介質(zhì)由于粒徑分布均勻可以確保柱與柱的一致性和穩定性���。
第二��,在連續層析過(guò)程中�����,使用的是串聯(lián)的小柱子���,為了提高生產(chǎn)效率�,線(xiàn)性流速要快�,這就對層析介質(zhì)機械強度要求更高�,以滿(mǎn)足高流速下產(chǎn)生的高壓力���。目前市場(chǎng)上主流的介質(zhì)是軟膠�,耐壓性差���,只能低流速操作�。納微新型單分散層析介質(zhì)由于是高度交聯(lián)的介質(zhì)�,因此機械強度高���,可滿(mǎn)足高流速的需求�����。
第三�,層析介質(zhì)的實(shí)際有效載量與純化效率也有直接的關(guān)系��,實(shí)際有效載量是指介質(zhì)在實(shí)際生產(chǎn)條件尤其是流動(dòng)相速度下的載量����。實(shí)際有效載量越高����,樣品上樣量可以越大�。但線(xiàn)性流速越快����,柱保留時(shí)間越短�����,則實(shí)際有效載量越低����。軟膠雖然在低流速下有較高載量��,但在高流速下�����,載量迅速下降�����。單分散聚合物層析介質(zhì)是大孔結構的微球����,通透性好�,蛋白在微球內的傳遞速度快��,因此在高流速下能保持較高的載量����。因此粒徑均一(單分散)��,高機械強度����,高流速下保持高載量的介質(zhì)是連續層析生產(chǎn)的理想的介質(zhì)����。連續層析技術(shù)是實(shí)現連續生產(chǎn)的關(guān)鍵技術(shù)����。連續生產(chǎn)制藥技術(shù)是一種新興技術(shù)�����,雖然還面臨著(zhù)許多監管的問(wèn)題和技術(shù)的挑戰��,但連續生產(chǎn)的優(yōu)越性卻顯而易見(jiàn)�����,也是生物制藥工藝發(fā)展的趨勢之一����。
隨著(zhù)多個(gè)重磅原研生物藥的專(zhuān)利到期���,為了滿(mǎn)足臨床市場(chǎng)的需求和降低原研生物藥的昂貴醫療費用�����,越來(lái)越多的制藥企業(yè)進(jìn)入生物類(lèi)似藥的開(kāi)發(fā)領(lǐng)域����,這進(jìn)一步加劇了生物類(lèi)似藥的競爭��,企業(yè)成本壓力日益凸顯��?��?贵w的主要成本在于下游的分離純化�����,而Protein A 親和層析成本占據整個(gè)層析分離純化的80%以上����,也是下游分離純化的瓶頸�����,因此��,實(shí)現Protein A親和層析介質(zhì)國產(chǎn)化�����,并通過(guò)底層技術(shù)創(chuàng )新改善Protein A 機械強度�����,傳質(zhì)速度及耐堿性能���,開(kāi)發(fā)出新一代單分散Protein A親和層析介質(zhì)�����,使其可以在高流速下純化抗體以提高生產(chǎn)效率�,降低成本生產(chǎn)�����。另外機械強度高及傳質(zhì)快的Protein A 介質(zhì)又有利于創(chuàng )新連續層析及高柱床的工藝實(shí)施���,進(jìn)一步提高抗體的生產(chǎn)效率和降低抗體生產(chǎn)成本���,也為中國生物制藥發(fā)展實(shí)現后發(fā)優(yōu)勢提供支撐��。